Por Tiana Quevedo
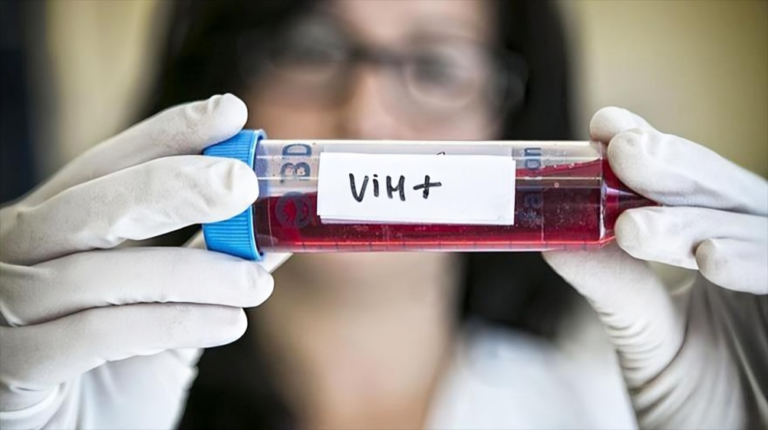
El gobierno de Colombia dio un paso trascendental al expedir la primera licencia obligatoria de su historia. La decisión la tomó con el fin de superar las barreras de las patentes al tratamiento del VIH en el país e importar versiones genéricas menos costosas del medicamento dolutegravir, sin permiso de los titulares de la patente SHIONOGI & CO., LTD. y VIIV HEALTHCARE COMPANY, decisión que no constituye una expropiación de la patente, ni una violación a los derechos del titular de esta, pues la licencia obligatoria no impide que el mismo la pueda seguir explotando.
La Ley 972 subraya la obligación del Estado colombiano de mejorar la atención a la población que sufre enfermedades catastróficas como el VIH/SIDA por medio de: “[…] ‘el suministro de los medicamentos, reactivos y dispositivos médicos autorizados“. La declaratoria de interés público en la modalidad de uso gubernamental, respaldada por la Resolución 1579, justifica la licencia obligatoria de la patente, ya que “la accesibilidad a medicamentos es una razón válida de interés público que justifica el otorgamiento de una licencia obligatoria […] con el objeto de proteger de manera permanente la vida y salud de los ciudadanos […]”. Así, la concesión de esta licencia permitirá la importación y disponibilidad del medicamento genérico, posibilitando el acceso al tratamiento con dolutegravir para personas que viven con VIH. Esta medida, respaldada por el Ministerio de Salud y Protección Social, busca evitar un impacto mayor en la propagación de la epidemia a nivel nacional. Además, este fármaco, recomendado por la OMS y la Guía Práctica Clínica de Colombia 2021, destaca por su eficacia, facilidad de administración, menor cantidad de efectos secundarios y alta barrera a la farmacorresistencia, convirtiéndolo en la opción preferida para el tratamiento del VIH.
El 31 de enero último en Colombia, la Superintendencia de Industria y Comercio publicó, a manera de convocatoria, que recibirán solicitudes para la licencia obligatoria referente a la patente N° 1887, que abarca el compuesto activo dolutegravir. Se establecieron los términos y condiciones para los interesados, permitiendo el suministro de dolutegravir en presentación de monofármaco o combinaciones a dosis fijas, siempre que los compuestos activos no estén protegidos por una patente vigente en Colombia. Además, la totalidad del medicamento bajo esta licencia debe destinarse al uso gubernamental, siendo exclusivamente proveído al Ministerio; y las etiquetas y paquetes de los productos fabricados deben llevar una leyenda que especifique tal condición o exclusividad.
La duración de la licencia será efectiva a partir de la fecha de ejecutoria del acto administrativo que la otorgue y se mantendrá mientras la patente esté vigente y existan razones de interés público, cumpliendo las condiciones establecidas. En todo caso, la duración de la licencia no excederá del 28 de abril de 2026.
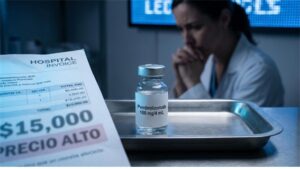
Finalmente, la compensación económica, fijada en un 3,50% del valor del producto genérico, implica que cualquier titular de la licencia deberá comprometerse a pagar a los titulares de la patente, un monto de $0,11 pesos colombianos por cada miligramo de dolutegravir introducido o producido en el país para uso gubernamental. Este pago se realizará periódicamente durante la vigencia de la licencia, incluyendo impuestos directos e indirectos. El cálculo del monto se basará en el reporte del sistema de información del Ministerio de Salud , entidad rectora del sector salud, según la normativa vigente.
Referencias:
- Presentación solicitudes de licencia obligatoria por razones de interés público en modalidad de uso gubernamental. | Sede Electronica [Internet]. Sic.gov.co. 2024 [cited 2024 Feb 5]. Available from: https://sedeelectronica.sic.gov.co/noticias/presentacion-solicitudes-de-licencia-obligatoria-por-razones-de-interes-publico-en-modalidad-de-uso-gubernamental