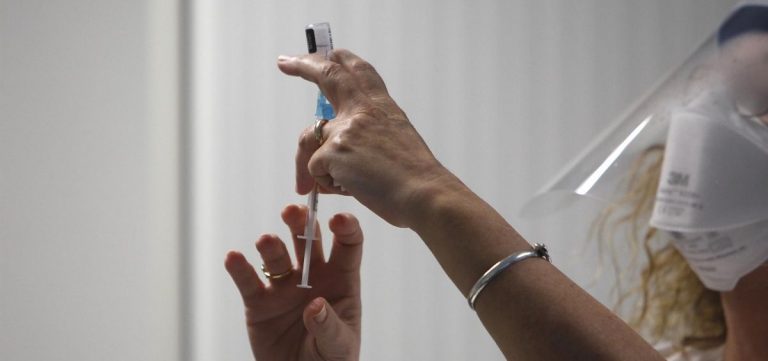
España, 09 de julio de 2021. El Comité para la Evaluación de Riesgos de Farmacovigilancia Europeo (PRAC) ha concluido que tras la administración de las vacunas Comirnaty (BioNtech/Pfizer) y Spikevax (Moderna) puede presentarse muy raramente miocarditis y/o pericarditis. En su revisión se ha analizado toda la información disponible, incluyendo los casos notificados en el Espacio Económico Europeo y los datos procedentes de la notificación en otros países.
Los casos aparecen fundamentalmente dentro de los 14 días siguientes a la vacunación, más frecuentemente después de la segunda dosis y en hombres jóvenes. La información disponible indica que el curso clínico es similar al observado habitualmente en la población por cualquier otra causa, mejorando con reposo y tratamiento farmacológico.
EL PRAC no ha establecido relación causal de miocarditis o pericarditis con las otras dos vacunas disponibles (COVID-19 Vaccine Janssen y Vaxzevria).
El Sistema Español de Farmacovigilancia (SEFV-H) ha registrado hasta el 4 de julio de 2021, 49 notificaciones de miocarditis o pericarditis tras la administración de Comirnaty y 12 tras la administración de Spikevax. En la mayoría de ellas los pacientes se habían recuperado o estaban en recuperación en el momento de la notificación al SEFV-H. En un caso notificado, el paciente falleció, tratándose de un paciente mayor de 60 años que presentaba causas alternativas que se han asociado con la aparición de miocarditis. A esa misma fecha, se habían administrado en España más de 30 millones de dosis de Comirnaty y aproximadamente 4 millones de dosis de Spikevax.
Los síntomas de miocarditis/pericarditis son variables, y frecuentemente incluyen dificultad para respirar, palpitaciones que pueden acompañarse de ritmo cardiaco irregular y dolor precordial. Estas condiciones habitualmente mejoran por sí solas o con el tratamiento adecuado.
El balance beneficio/riesgo de Comirnaty y Spikevax se mantiene favorable considerando la alta eficacia de estas vacunas en prevenir hospitalizaciones y muertes por COVID-19 y la baja frecuencia de aparición de estos cuadros, de curso generalmente benigno.
Las fichas técnicas y prospectos de estas dos vacunas se actualizarán para reflejar esta información y se continuará vigilando estrechamente este asunto para todas las vacunas frente a la COVID-19. La AEMPS comunicará cualquier nueva información relevante sobre este asunto.