En setiembre de este año, organizaciones de la sociedad civil solicitaron al gobierno peruano declarar de interés público el medicamento compuesto por elexacaftor, ivacaftor y tezacaftor indicado en el tratamiento de la fibrosis quística. De acuerdo con nuestra normatividad nacional, dicha declaración es el requisito esencial para otorgar una licencia obligatoria que promueve la competencia, permitiendo la entrada de productos genéricos. Actualmente, el medicamento se comercializa con el nombre de Trikafta®, con patente hasta el año 2039 y a precios monopólicos, que pone en riesgo la sostenibilidad de los tratamientos.
En Perú, son más de 100 pacientes con la mencionada enfermedad que pertenecen al Seguro Integral de Salud (SIS) y a la seguridad social (ESSALUD). En diciembre de 2024, el MINSA adjudicó por primera vez la compra de 6,0481 tabletas de Trikafta® por un valor de S/816.50 por tableta, lo que equivale a S/823,032 el tratamiento por persona/año. En enero de 2025 se inició el tratamiento de 12 personas por un período de 6 meses, obligando al Ministerio de Salud a realizar nuevas compras para dar continuidad al tratamiento.
El alto precio de este medicamento es una barrera para el acceso a nivel global. En varios países han implementado iniciativas para mejorar el precio y dar tratamiento a más pacientes, como la realizada por Just treatment2 que ha logrado mejorar la negociación de precios a través de acciones de incidencia en Brasil, Sudáfrica, Estonia y Lithuana, entre otros.
La licencia obligatoria es un instrumento contemplado en el Acuerdo sobre los Derechos de Propiedad Intelectual Relacionados al Comercio (ADPIC) y permite importar o producir localmente versiones genéricas existiendo patente. El uso de este instrumento es una facultad que tienen los gobiernos para proteger el interés público.
La versión genérica de Trikafta® se produce en Argentina, país que paga aproximadamente S/ 162,000 por paciente/año, lo que equivale a 80% menos del precio pagado en Perú.
Las licencias obligatorias en países de Latinoamérica como Brasil, Ecuador, y recientemente Colombia han tenido resultados exitosos. En 2023, Colombia otorgó la licencia obligatoria para dolutegravir, medicamento usado en el VIH/SIDA, logrando una reducción de 96% del precio, permitiendo tratar a más pacientes, y disminuir la carga financiera sobre las instituciones prestadoras de atención médica.
Compras recientes
En setiembre 2025 el MINSA adquirió 5,376 tabletas a un precio de S/783.93 por tableta. El precio es 4.8% menos de lo pagado en la primera compra.

En agosto 2025 EsSALUD adquirió dos presentaciones diferentes de la combinación elexacaftor, ivacaftor y tezacaftor, adquirida por el MINSA.
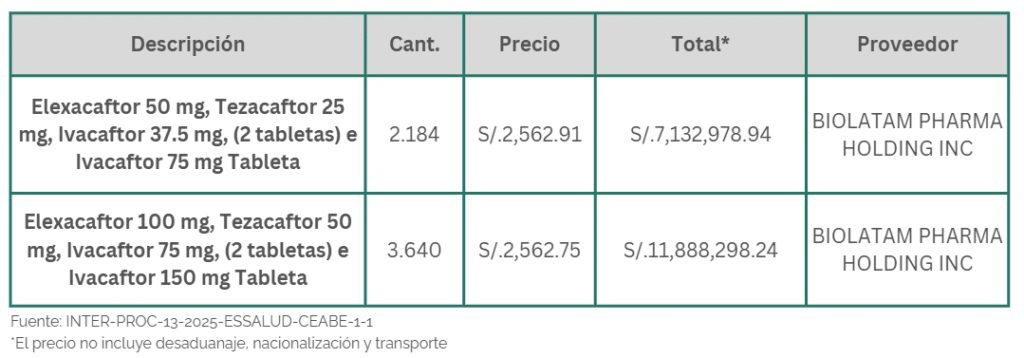
En los últimos dos meses se ha comprado Tricafta® por un valor de S/. 23,235,277.18 entre ambas instituciones. Las compras se hicieron al mismo proveedor, con diferencias significativas en el precio teniendo en cuenta las diferentes presentaciones (la presentación de Elexacaftor 100 mg, Tezacaftor 50 mg, Ivacaftor 75 mg, (2 tabletas) e Ivacaftor 150 mg Tableta de EsSalud es cerca del doble de la presentación del MINSA. Sin embargo, el precio es más de tres veces comparado con el MINSA).
Las organizaciones de la sociedad civil esperan una pronta respuesta del MINSA, solicitando tomar en cuenta las lecciones de otros países para obtener precios convenientes, sustentados si es necesario, por las licencias obligatorias.
Referencias:
[1]INTER-PROC-14-2024-CENARES/MINSA-1
[2]https://justtreatment.org/